Skandiumi, mille elemendi tähis on Sc ja aatomnumber 21, on vees kergesti lahustuv, võib reageerida kuuma veega ja tumeneb õhus kergesti. Selle peamine valents on +3. Seda segatakse sageli gadoliiniumi, erbiumi ja teiste elementidega, mille saagis on madal ja sisaldus maakoores on umbes 0,0005%. Skandiumi kasutatakse sageli spetsiaalse klaasi ja kergete kõrgtemperatuuriliste sulamite valmistamiseks.
Praegu on maailma tõestatud skandiumi varud vaid 2 miljonit tonni, millest 90–95% sisaldub boksiidi-, fosforiidi- ja raud-titaanimaakides ning väike osa uraani-, tooriumi-, volframi- ja haruldaste muldmetallide maakides, mis asuvad peamiselt Venemaal, Hiinas, Tadžikistanis, Madagaskaril, Norras ja teistes riikides. Hiina on skandiumi ressursside poolest väga rikas, seal on tohutud skandiumiga seotud maavarade varud. Mittetäieliku statistika kohaselt on Hiina skandiumi varud umbes 600 000 tonni, mis sisalduvad boksiidi ja fosforiidi leiukohtades, porfüüri ja kvartsveenide volframi leiukohtades Lõuna-Hiinas, haruldaste muldmetallide leiukohtades Lõuna-Hiinas, Bayan Obo haruldaste muldmetallide rauamaagi leiukohas Sise-Mongoolias ja Panzhihua vanaadiumi-titaanmagnetiidi leiukohas Sichuanis.
Skandiumi nappuse tõttu on ka skandiumi hind väga kõrge ja oma tipphetkel oli skandiumi hind 10 korda kõrgem kui kulla hind. Kuigi skandiumi hind on langenud, on see ikkagi neli korda kõrgem kui kulla hind!
Ajaloo avastamine
1869. aastal märkas Mendelejev kaltsiumi (40) ja titaani (48) aatommassi erinevust ning ennustas, et siin on ka avastamata vahepealne aatommassiga element. Ta ennustas, et selle oksiid on X ₂ O Å. Skandiumi avastas 1879. aastal Lars Frederik Nilson Uppsala ülikoolist Rootsis. Ta kaevandas selle mustast haruldasest kullakaevandusest, mis on keeruline maak, mis sisaldab 8 tüüpi metallioksiide. Ta on kaevandanudErbium(III) oksiidmustast haruldasest kullamaagist ja saadudÜtterbium(III) oksiidsellest oksiidist ja on olemas veel üks kergema elemendi oksiid, mille spekter näitab, et see on tundmatu metall. See on Mendelejevi ennustatud metall, mille oksiid onSc₂O₃Skandiummetall ise toodetiSkandiumkloriidelektrolüütilise sulatamise teel 1937. aastal.
Mendelejev
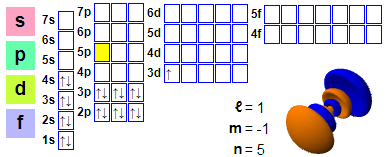
Elektronkonfiguratsioon
Elektronkonfiguratsioon: 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Skandium on pehme, hõbevalge siirdemetall, mille sulamistemperatuur on 1541 ℃ ja keemistemperatuur 2831 ℃.
Pärast skandiumi avastamist ei olnud selle kasutamist pikka aega demonstreeritud selle tootmise keerukuse tõttu. Haruldaste muldmetallide eraldamismeetodite pideva täiustumisega on nüüd olemas küps protsess skandiumiühendite puhastamiseks. Kuna skandium on vähem aluseline kui ütrium ja lantanoidid, on hüdroksiid kõige nõrgem, seega eraldatakse skandiumi sisaldav haruldaste muldmetallide segumineraal haruldastest muldmetallidest "astmelise sadestamise" meetodil, kui skandium(III) hüdroksiidi töödeldakse pärast lahusesse viimist ammoniaagiga. Teine meetod on skandiumnitraadi eraldamine nitraadi polaarse lagundamise teel. Kuna skandiumnitraat on kõige kergemini lagunev, saab skandiumi eraldada. Lisaks on skandiumi oluline allikas ka kaasneva skandiumi ulatuslik eraldamine uraanist, tooriumist, volframist, tinast ja muudest mineraalide leiukohtadest.
Pärast puhta skandiumiühendi saamist muundatakse see ScCl Å-ks ja sulatatakse koos KCl ja LiCl-iga. Sula tsinki kasutatakse elektrolüüsi katoodina, mis põhjustab skandiumi sadestumist tsinkelektroodile. Seejärel aurustatakse tsink, et saada metalliline skandium. See on kerge hõbevalge metall, millel on väga aktiivsed keemilised omadused ja mis reageerib kuuma veega, moodustades vesinikgaasi. Seega on pildil olev metalliline skandium pudelis suletud ja kaitstud argoongaasiga, vastasel juhul moodustab skandium kiiresti tumekollase või halli oksiidikihi, kaotades oma läikiva metallilise läike.
Rakendused
Valgustustööstus
Skandiumi kasutusalad on koondunud väga eredatesse suundadesse ja pole liialdus seda nimetada Valguse Pojaks. Skandiumi esimene maagiline relv on skandiumnaatriumlamp, mida saab kasutada tuhandete majapidamiste valgustamiseks. See on metallhalogeniidlamp: pirn on täidetud naatriumjodiidi ja skandiumtrijodiidiga ning samal ajal lisatakse skandium ja naatriumfoolium. Kõrgepinge tühjenemise ajal kiirgavad skandiumioonid ja naatriumioonid vastavalt oma iseloomulikel emissioonlainepikkustel valgust. Naatriumi spektraaljooned on 589,0 ja 589,6 nm, mis on kaks kuulsat kollast valgust, samas kui skandiumi spektraaljooned on 361,3–424,7 nm, mis on lähiultraviolettkiirguse ja sinise valguse emissioonide seeria. Kuna need üksteist täiendavad, on tekkiv valgusvärv valge. Just seetõttu, et skandiumnaatriumlampidel on kõrge valgusviljakus, hea valguse värvus, energiasäästlikkus, pikk kasutusiga ja tugev udu hajumise võime, saab neid laialdaselt kasutada telekaamerate, väljakute, spordirajatiste ja teede valgustuses ning neid tuntakse kolmanda põlvkonna valgusallikatena. Hiinas hakatakse seda tüüpi lampi järk-järgult uue tehnoloogiana propageerima, samas kui mõnes arenenud riigis kasutati seda tüüpi lampi laialdaselt juba 1980. aastate alguses.
Skandiumi teine võlurelv on päikesepaneelid, mis suudavad koguda maapinnale hajutatud valgust ja muuta selle inimühiskonna elektrienergiaks. Skandium on parim barjäärmetall metall-isolaatoris, pooljuht-räni päikesepatareides ja päikesepatareides.
Selle kolmandat maagilist relva nimetatakse γA-kiirgusallikaks. See maagiline relv võib iseenesest eredalt särada, kuid seda tüüpi valgust ei ole palja silmaga võimalik näha, see on suure energiaga footonivoog. Tavaliselt ekstraheerime 45Sc mineraalidest, mis on skandiumi ainsad looduslikud isotoobid. Iga 45Sc tuum sisaldab 21 prootonit ja 24 neutronit. 46Sc, kunstlik radioaktiivne isotoop, saab kasutada γ-kiirgusallikana või märgistusaatomitena, mida saab kasutada ka pahaloomuliste kasvajate kiiritusravis. On ka rakendusi nagu ütrium-gallium-skandium-granaatlaser.Skandiumfluoriidklaasist infrapunakiudoptika ja skandiumiga kaetud elektronkiiretoru televisioonis. Näib, et skandium sünnib heledusega.
Sulamistööstus
Skandiumi elementvormi on laialdaselt kasutatud alumiiniumisulamite legeerimiseks. Niikaua kui alumiiniumile lisatakse paar tuhandikku skandiumi, moodustub uus Al3Sc faas, mis mängib alumiiniumisulamis metamorfismi rolli ning muudab oluliselt sulami struktuuri ja omadusi. 0,2%–0,4% Sc lisamine (mis on tegelikult sarnane soola lisamise osakaaluga kodus praetud köögiviljadele, vaja on vaid väikest kogust) võib tõsta sulami rekristallisatsioonitemperatuuri 150–200 ℃ võrra ning parandada oluliselt kõrgtemperatuurilist tugevust, konstruktsiooni stabiilsust, keevitusomadusi ja korrosioonikindlust. Samuti aitab see vältida hapruse nähtust, mis on pikaajalisel kõrgel temperatuuril töötamisel kergesti tekkiv. Kõrge tugevusega ja suure sitkusega alumiiniumisulam, uus kõrge tugevusega korrosioonikindel keevitatav alumiiniumisulam, uus kõrge temperatuuriga alumiiniumisulam, kõrge tugevusega neutronkiirgusele vastupidav alumiiniumisulam jne pakuvad väga atraktiivseid arenguvõimalusi lennunduses, laevadel, tuumareaktorites, kergsõidukites ja kiirrongides.
Skandium on suurepärane ka raua modifitseerija ning väike kogus skandiumi võib oluliselt parandada malmi tugevust ja kõvadust. Lisaks saab skandiumi kasutada ka lisandina kõrge temperatuuriga volframi- ja kroomisulamites. Loomulikult on skandiumil lisaks pulmarõivaste valmistamisele ka kõrge sulamistemperatuur ja selle tihedus on sarnane alumiiniumiga ning seda kasutatakse ka kõrge sulamistemperatuuriga kergsulamistes, nagu skandium-titaanisulamist ja skandium-magneesiumisulamitest. Kõrge hinna tõttu kasutatakse seda aga üldiselt ainult tipptasemel tootmistööstuses, näiteks kosmosesüstikutes ja rakettides.
Keraamiline materjal
Skandiumi kui ainet kasutatakse tavaliselt sulamites ja selle oksiidid mängivad sarnast olulist rolli ka keraamilistes materjalides. Tetragonaalsel tsirkooniumkeraamilisel materjalil, mida saab kasutada tahkeoksiidkütuseelementide elektroodimaterjalina, on ainulaadne omadus, mille kohaselt selle elektrolüüdi juhtivus suureneb temperatuuri ja hapniku kontsentratsiooni tõustes keskkonnas. Selle keraamilise materjali kristallstruktuur ise ei saa aga stabiilselt eksisteerida ja sellel puudub tööstuslik väärtus; selle algsete omaduste säilitamiseks on vaja lisada mõningaid aineid, mis seda struktuuri fikseerivad. 6–10% skandiumoksiidi lisamine on nagu betoonstruktuur, mis võimaldab tsirkooniumoksiidi stabiliseerida ruudukujulisele võrele.
Samuti on olemas insenerikeraamilised materjalid, näiteks ülitugev ja kõrgele temperatuurile vastupidav räninitriid tihendajatena ja stabilisaatoritena.
TihendajanaSkandiumoksiidSee võib moodustada peenosakeste servas tulekindla faasi Sc2Si2O7, vähendades seeläbi insenerkeraamika kõrgel temperatuuril deformeerumist. Võrreldes teiste oksiididega parandab see räninitriidi kõrgel temperatuuril mehaanilisi omadusi.
Katalüütiline keemia
Keemiatehnikas kasutatakse skandiumi sageli katalüsaatorina, samas kui Sc2O3 saab kasutada etanooli või isopropanooli dehüdratsiooniks ja deoksüdatsiooniks, äädikhappe lagundamiseks ning etüleeni tootmiseks CO-st ja H2-st. Sc2O3 sisaldav PtAl katalüsaator on oluline katalüsaator ka naftakeemiatööstuse raskete õlide hüdrogeenimisel, puhastamisel ja rafineerimisel. Katalüütilise krakkimise reaktsioonides, näiteks kumeenis, on Sc-Y tseoliitkatalüsaatori aktiivsus 1000 korda suurem kui alumiiniumsilikaatkatalüsaatoril; võrreldes mõnede traditsiooniliste katalüsaatoritega on skandiumkatalüsaatorite arenguväljavaated väga head.
Tuumaenergia tööstus
Väikese koguse Sc2O3 lisamine UO2-le kõrgtemperatuurilises reaktori tuumkütuses aitab vältida võre muutumist, mahu suurenemist ja pragunemist, mis on põhjustatud UO2 muundumisest U3O8-ks.
Kütuseelement
Samamoodi pikendab nikkel-leelispatareidele 2,5–25% skandiumi lisamine nende kasutusiga.
Põllumajanduslik aretus
Põllumajanduses saab skandiumsulfaadiga töödelda selliseid seemneid nagu mais, peet, hernes, nisu ja päevalill (kontsentratsioon on üldiselt 10-3–10-8 mol/l, erinevatel taimedel on erinev mõju) ning tegelik idanemist soodustav efekt on saavutatud. 8 tunni pärast suurenes juurte ja pungade kuivmass vastavalt 37% ja 78% võrreldes seemikutega, kuid mehhanismi uuritakse veel.
Nielseni tähelepanust aatommassi andmete võlgadele tänapäevani on skandium inimeste nägemusse jõudnud vaid sada või kakskümmend aastat, kuid see on peaaegu et sada aastat pingil seisnud. Alles materjaliteaduse jõuline areng eelmise sajandi lõpus andis see talle elujõudu. Tänapäeval on haruldased muldmetallid, sealhulgas skandium, saanud materjaliteaduse kuumadeks tähtedeks, mängides pidevalt muutuvat rolli tuhandetes süsteemides, tuues meie ellu iga päev rohkem mugavust ja luues majanduslikku väärtust, mida on veelgi raskem mõõta.
Postituse aeg: 29. juuni 2023